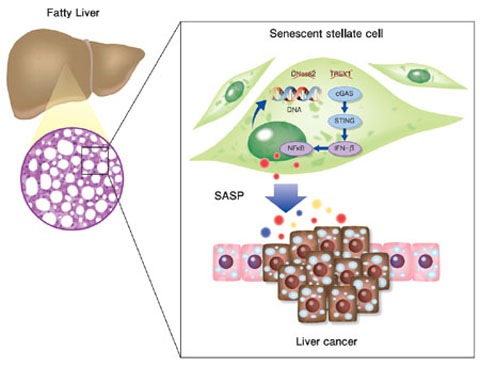
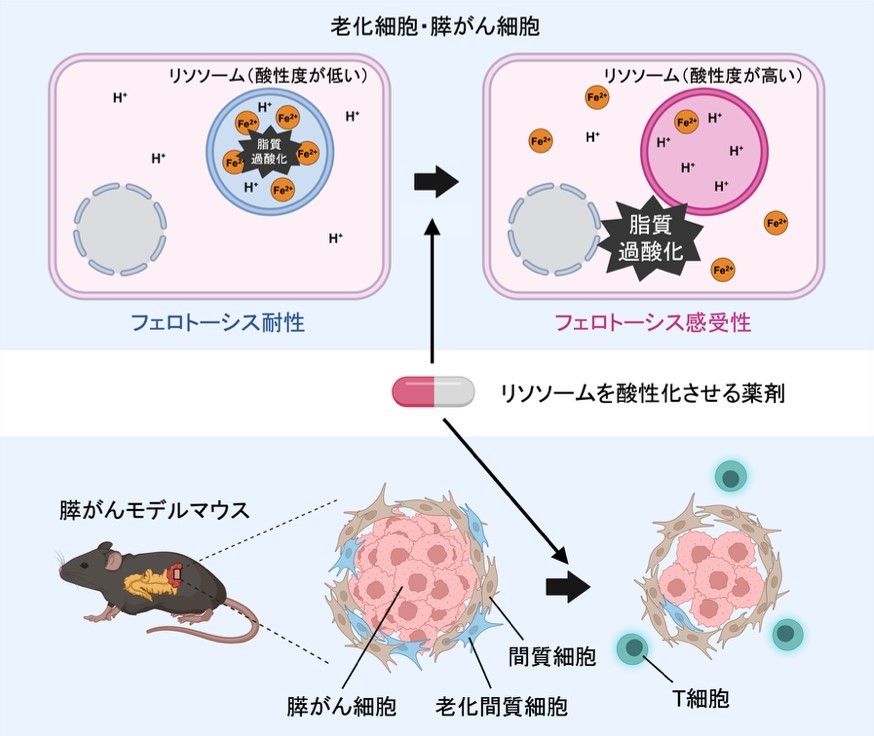
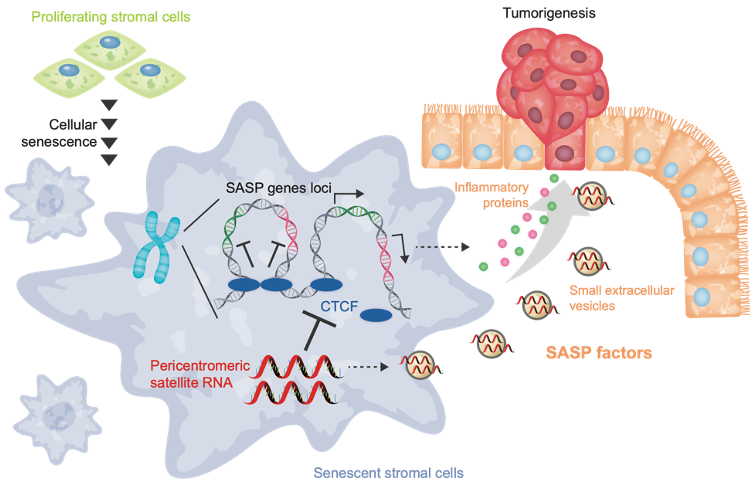
私たちの体を構成する細胞は加齢と伴に「細胞老化」をおこします。 細胞が老化する原因はあらゆるストレスであり、細胞老化がおこると細胞の増殖は不可逆的に停止します(Takahashi et al., Nat Cell Biol, 2006: Imai et al., Cell Rep, 2014)。 がん遺伝子の活性化や酸化的ストレスなどの発がんストレスも細胞老化を引き起こす原因の一つであり(Takahashi, , Nat Rev MCB, 2024)、近年では抗がん剤や放射線などのがんの治療やウイルス感染も細胞老化を促進することが知られています(Yamauchi et al., J Biochem, 2025)。私たちは、個体老化や肥満などのストレスによって老化細胞が体内に蓄積してゆくことを 老化細胞イメージングマウスや老化細胞特異的酵素活性プローブを用いた研究で明らかにしてきました(Yamakoshi & Takahashi et al., JCB, 2009; Tanaka et al., Cancer Sci, 2024)。細胞老化は生体内で異常な細胞の増殖を止めるがん抑制機構として働く一方で、発がんを促進する負の側面があることもわかってきました(Loo et al., Cancer Sci, 2020)。
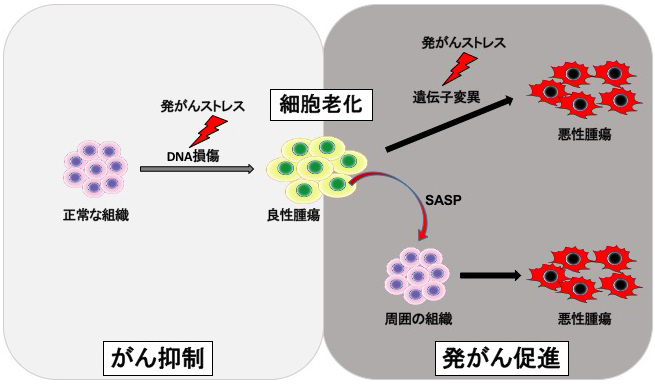
出典:細胞工学2015年